Đề Ôn Thi Tốt Nghiệp THPT 2023 Môn Hóa Học Online-Đề 3
Chủ đề:Trắc Nghiệm Online Môn Hóa
Ghi chú: Bạn có thể xem thêm phiên bản đầy đủ của đề thi này và các tài liệu liên quan tại đường dẫn:https://tusach.vn/tai-lieu-hoc-tap/trac-nghiem/de-on-thi-tot-nghiep-thpt-2023-mon-hoa-hoc-online-de-3
Đề Kiểm Tra: Đề Ôn Thi Tốt Nghiệp THPT 2023 Môn Hóa Học Online-Đề 3
Câu 1:
Chất nào sau đây là chất điện li mạnh?
C6H12O6.
Câu 2:
X là một hợp chất hữu cơ có khả năng làm quỳ tím chuyển xanh và có công thức cấu tạo: H2N-(CH2)4-CH(NH2)-COOH. Tên gọi của X là?
axit glutamic.
Câu 3:
Kim loại nào sau đây là kim loại kiềm thổ?
Na.
Câu 4:
Phân urê có công thức hóa học là
KNO3.
Câu 5:
Polime nào sau đây có cấu trúc mạch phân nhánh?
Amilopectin.
Câu 6:
Chất nào sau đây tác dụng được với dung dịch KOH?
HCl.
Câu 7:
Trong công nghiệp, có thể chuyển hóa trực tiếp từ chất bẻo lỏng sang chất béo rắn bằng phản ứng
hiđro hóa.
Câu 8:
Kim loại nào sau đây phản ứng được với dung dịch H2SO4 đặc, nguội?
Cr.
Câu 9:
Kim loại Fe không phản ứng với dung dịch
NaNO3.
Câu 10:
Ở nhiệt độ thường, chất nào sau đây tạo kết tủa trắng khi tác dụng với dung dịch Br2?
Benzen.
Câu 11:
Kim loại nào sau đây thường được dùng trong các dây dẫn điện?
Sắt.
Câu 12:
Công thức của sắt (II) oxit là
FeO.
Câu 13:
Chất nào sau đây không có tính lưỡng tính?
AlCl3.
Câu 14:
Este X được tạo bởi ancol metylic và axit axetic. Công thức của X là
HCOOC2H5.
Câu 15:
Chất nào sau đây tham gia được phản ứng tráng bạc?
Glyxin.
Câu 16:
Saccarozơ là một loại đisaccarit có nhiều trong cây mía, hoa thốt nốt, củ cải đường. Trong thức phân tử của saccarozơ có bao nhiêu nguyên tử oxi
10.
Câu 17:
Kim loại nào sau đây tác dụng được với H2O ở nhiệt độ thường?
Be.
Câu 18:
Chất nào sau đây tạo kết tủa với dung dịch BaCl2 ở điều kiện thường
HCl.
Câu 19:
Quặng nào sau đây có chứa nguyên tố Fe?
Sinvinit.
Câu 20:
Trong các chất: Mg(OH)2, Al, NaHCO3 và Al(OH)3, số chất tác dụng với HCl và NaOH là
2.
Câu 21:
Thủy phân hoàn toàn 8,8 gam este C4H8O2 thu được 6 gam ancol. Công thức của X là
CH3COOCH3.
Câu 22:
Cho các phát biểu sau:
(a) Oxi hóa glucozơ thu được sobitol.
(b) Trong phân tử fructozơ có một nhóm -CHO.
(c) Xenlulozơ trinitrat được dùng làm thuốc súng không khói.
(d) Trong phân tử xenlulozơ, mỗi gốc glucozơ có ba nhóm -OH.
Số phát biểu đúng là
(a) Oxi hóa glucozơ thu được sobitol.
(b) Trong phân tử fructozơ có một nhóm -CHO.
(c) Xenlulozơ trinitrat được dùng làm thuốc súng không khói.
(d) Trong phân tử xenlulozơ, mỗi gốc glucozơ có ba nhóm -OH.
Số phát biểu đúng là
1.
Câu 23:
Cho 16,1 gam hỗn hợp X gồm CaCO3 và MgCO3 (có tỉ lệ mol 1:1) tan hết trong dung dịch HCl dư, thu được V lít (đktc) khí CO2. Giá trị của V là
2,94.
Câu 24:
Lên men một lượng glucozơ, thu được a mol ancol etylic và 0,1 mol CO2. Giá trị của a là
0,10.
Câu 25:
Chất X tác dụng với dung dịch HCl tạo ra dung dịch chứa hai muối, chất Y (lượng dư) tác dụng với dung dịch FeCl3 tạo ra dung dịch chứa một muối. Công thức của X, Y là
Fe(OH)3, Cu.
Câu 26:
Cho các polime sau: polietilen, tơ nilon-6, thủy tinh hữu cơ plexiglas, tơ nitron, cao su buna, poli vinylclorua. Số polime có chứa nguyên tố oxi trong phân tử là
2.
Câu 27:
Cho 5,6 gam Fe tác dụng hết với dung dịch HNO3 đặc, nóng(dư), sinh ra V lít khí NO2 (ở đktc, sản phẩm khử duy nhất). Giá trị của V là
2,24
Câu 28:
Hợp chất X là một \(\alpha \)-amino axit. Cho 0,01 mol X tác dụng vừa đủ với 80 ml dung dịch HCl 0,125M, sau đó đem cô cạn dung dịch thu được 1,835 gam muối. Phân tử khối của X là.
147.
Câu 29:
Đốt cháy hoàn toàn 0,5 mol hỗn hợp X gồm ba este A, B, C (MA < MB < MC, số mol nB > nC) đều mạch hở với lượng oxi vừa đủ, thu được 2,2 mol CO2 và 1,7 mol H2O. Mặt khác, hidro hóa hoàn toàn 0,5 mol X cần dùng a mol H2 (xúc tác Ni, t°) thu được hỗn hợp Y gồm hai este. Đun nóng toàn bộ Y với 700 ml dung dịch NaOH 1M (vừa đủ), thu được một muối của axit hữu cơ có tráng bạc và hỗn hợp Z gồm hai ancol có cùng số nguyên tử cacbon. Giá trị a và phần trăm khối lượng chất B trong X lần lượt là
0,3 và 33,72%.
Câu 30:
Cho khí CO dư đi qua 24 gam hỗn hợp X gồm CuO, Fe2O3 và MgO nung nóng, thu được m gam chất rắn Y và hỗn hợp khí Z. Dẫn từ từ toàn bộ khí Z vào 0,2 lít dung dịch gồm Ba(OH)2 1M và NaOH 1M, thu được 29,55 gam kết tủa, lọc kết tủa rồi đun nóng dung dịch lại thấy có kết tủa xuất hiện. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
17.
Câu 31:
Thực hiện chuỗi phản ứng sau (đúng với tỉ lệ mol các chất):
(a) \(X + 2NaOH\xrightarrow{{t^\circ }}{X_1} + 2{X_3}\).
(b) \({X_1} + 2NaOH\xrightarrow{{CaO,t^\circ }}{X_4} + 2N{a_2}C{O_3}\).
(c) \({C_6}{H_{12}}{O_6}\left( {{\text{glucozơ}}} \right)\xrightarrow{{{\text{lên men}}}}2{C_2}{H_5}OH\left( {{X_3}} \right) + 2C{O_2}\).
(d) \({X_3}\xrightarrow{{{H_2}S{O_4},170^\circ C}}{X_4} + 2{H_2}O\).
Biết X có mạch cacbon không phân nhánh. Nhận định nào sau đây là đúng?
(a) \(X + 2NaOH\xrightarrow{{t^\circ }}{X_1} + 2{X_3}\).
(b) \({X_1} + 2NaOH\xrightarrow{{CaO,t^\circ }}{X_4} + 2N{a_2}C{O_3}\).
(c) \({C_6}{H_{12}}{O_6}\left( {{\text{glucozơ}}} \right)\xrightarrow{{{\text{lên men}}}}2{C_2}{H_5}OH\left( {{X_3}} \right) + 2C{O_2}\).
(d) \({X_3}\xrightarrow{{{H_2}S{O_4},170^\circ C}}{X_4} + 2{H_2}O\).
Biết X có mạch cacbon không phân nhánh. Nhận định nào sau đây là đúng?
Nhiệt độ sôi của X4 lớn hơn X3.
a) \(C{H_2} = C{\left( {COO{C_2}{H_5}} \right)_2}\left( X \right) + 2NaOH \to C{H_2} = C{\left( {COONa} \right)_2}\left( {{X_1}} \right) + 2{C_2}{H_5}OH\left( {{X_3}} \right)\)
(b) \(C{H_2} = C{\left( {COONa} \right)_2}\left( {{X_1}} \right) + 2NaOH\xrightarrow{{CaO,t^\circ }}{C_2}{H_4}\left( {{X_4}} \right) + 2N{a_2}C{O_3}\)
(c) \({C_6}{H_{12}}{O_6}\left( {{\text{glucozơ}}} \right)\xrightarrow{{{\text{lên men}}}}2{C_2}{H_5}OH\left( {{X_3}} \right) + 2C{O_2}\)
(d) \({C_2}{H_5}OH\left( {{X_3}} \right)\xrightarrow{{{H_2}S{O_{4{\text{ đặc}}}},170^\circ C}}{C_2}{H_4}\left( {{X_4}} \right) + {H_2}O\)
(b) \(C{H_2} = C{\left( {COONa} \right)_2}\left( {{X_1}} \right) + 2NaOH\xrightarrow{{CaO,t^\circ }}{C_2}{H_4}\left( {{X_4}} \right) + 2N{a_2}C{O_3}\)
(c) \({C_6}{H_{12}}{O_6}\left( {{\text{glucozơ}}} \right)\xrightarrow{{{\text{lên men}}}}2{C_2}{H_5}OH\left( {{X_3}} \right) + 2C{O_2}\)
(d) \({C_2}{H_5}OH\left( {{X_3}} \right)\xrightarrow{{{H_2}S{O_{4{\text{ đặc}}}},170^\circ C}}{C_2}{H_4}\left( {{X_4}} \right) + {H_2}O\)
Câu 32:
Hỗn hợp X gồm axit oleic, axit stearic và triglixerit Y. Đốt cháy hoàn toàn m gam hỗn hợp X cần vừa đủ 2,89 mol O2 thu được 2,04 mol CO2. Mặt khác m gam hỗn hợp X làm mất màu vừa đủ 12,8 gam brom trong CCl4. Nếu cho m gam hỗn hợp X phản ứng với dung dịch NaOH đun nóng (vừa đủ) thu glixerol và dung dịch chứa hai muối. Khối lượng của Y trong m gam hỗn hợp X là
17,72.
\(X\xrightarrow{{quy\,doi}}\left\{ \begin{gathered}{C_{17}}{H_{33}}COOH:0,08\,mol\left( {{n_{{C_{17}}{H_{33}}COOH}} = {n_{B{r_2}}} = \frac{{12,8}}{{160}} = 0,08} \right) \hfill \\{C_{17}}{H_{33}}COOH:a\,mol \hfill \\{C_3}{H_2}:b\,mol \hfill \\{H_2}:\,c\,mol \hfill \\\end{gathered} \right.\)\( \to \left\{ \begin{gathered}2,89 = \left( {18.0,08 + 18a + 3b} \right) + \frac{{34.0,08 + 36a + 2b}}{4} – \frac{{0,087.2 + 2a}}{2}\left( {{n_{{O_2}}} = {n_C} + \frac{{{n_H}}}{4} – \frac{{{n_O}}}{2}} \right) \hfill \\BT\left[ C \right]:18.0,08 + 18a + 3b = 2,04 \hfill \\\end{gathered} \right.\)\(\xrightarrow[{}]{{}}\left\{ \begin{gathered}a = 0,03 \hfill \\b = 0,02 = {n_Y} \hfill \\\end{gathered} \right. \to \frac{{{n_{{C_{17}}{H_{35}}COOH}}}}{{{n_Y}}} = 1,5 \to \) Y chỉ chứa 1 gốc stearat C17H35COO→ Y: (C17H35COO)(C17H33COO)2C3H5: 0,02mol \( \to {m_Y} = 17,72\,g\)
Câu 33:
Cho 0,1 mol Fe; 0,15 mol Fe (NO3)2 và m gam Al tan hết trong dung dịch HCl. Sau phản ứng thu được 2,352 lít (đktc) hỗn hợp khí X gồm NO và N2O có tỉ khối so với H2 là 16, dung dịch Y chỉ chứa 47,455 gam muối trung hòa. Cho NaOH dư vào Y thì thấy có 0,82 mol NaOH phản ứng. Biết các phản ứng hoàn toàn. Cho AgNO3 dư vào Y thu được bao nhiêu gam kết tủa?
98,335.
\({n_X} = 0,105 \to \left\{ \begin{gathered}NO:0,09 \hfill \\{N_2}O:0,015 \hfill \\\end{gathered} \right.\left\{ \begin{gathered}{n_{Al}} = a \hfill \\{n_{NH_4^ + }} = b \hfill \\n_{NO_3^ – }^{trong\,Y} = c \hfill \\\end{gathered} \right.\xrightarrow[{}]{{{H^ + }}}{n_{{H^ + }}} = {n_{C{l^ – }}} = {n_{HCl}} = 4{n_{NO}} + 10{n_{{N_2}O}} + 10{n_{NH_4^ + }} = 0,51 + 10b\)\(Y + NaOH \to \left\{ \begin{gathered}NaN{O_3}:c \hfill \\NaCl:0,51 + 10b \hfill \\NaAl{O_2}:a \hfill \\\end{gathered} \right. \to \left\{ \begin{gathered}0,15.2 = 0,09 + 0,015.2 + b + c\left( {BT:N} \right) \hfill \\a + \left( {10b + 0,51} \right) + c = 0,82\left( {BT:Na} \right) \hfill \\0,25.56 + 27a + 18b + 35,5\left( {0,51 + 10b} \right) + 62.c = 47,455 \hfill \\\end{gathered} \right. \to \left\{ \begin{gathered}a = 0,04 \hfill \\b = 0,01 \hfill \\c = 0,17 \hfill \\\end{gathered} \right.\)\(\xrightarrow[{}]{{BT:e}}{n_e} = 0,1.3 + 0,15 + 0,04.3 = 0,09.3 + 0,015.8 + 0,01.8 + {n_{Ag}} = 0,1\xrightarrow[{}]{{}}98,335\left\{ \begin{gathered}AgCl:0,61 \hfill \\Ag:0,1 \hfill \\\end{gathered} \right.\)
Câu 34:
Cho các phát biểu sau(a) Kim loại Cu oxi hóa được Fe3+ trong dung dịch.(b) Cho dung dịch NH3 vào dung dịch AlCl3 có xuất hiện kết tủa.(c) Hỗn hợp Na2O và Al (tỉ lệ mol 1 : 1) tan hết trong nước dư.(d) Trong công nghiệp dược phẩm, NaHCO3 được dùng đề điều chế thuốc đau dạ dày.(e) Cho viên Zn vào dung dịch HCl thì viên Zn bị ăn mòn hóa học.Số phát biểu đúng là
3
(a) Sai vì Cu khử Fe3+(b) Đúng vì tạo kết tủa Al(OH)3(c) Đúng vì nNaOH = 2(mol) > nAl = 1(mol) nên hỗn hợp tan hết, trong dung dịch gồm NaAlO2 và NaOH dư(d) Đúng(e) Đúng
Câu 35:
Cho sơ đồ sau: \(X\xrightarrow{{ + C{O_2} + {H_2}O}}Y\xrightarrow{{ + NaHS{O_4}}}Z\xrightarrow{{ + Ba{{\left( {OH} \right)}_2}}}T\xrightarrow{{ + Y}}X\). Các chất X và Z tương ứng là
Na2CO3 và NaOH.
\(N{a_2}C{O_3}\xrightarrow{{ + C{O_2} + {H_2}O}}NaHC{O_3}\xrightarrow{{ + NaHS{O_4}}}N{a_2}S{O_4}\xrightarrow{{ + Ba{{\left( {OH} \right)}_2}}}NaOH\xrightarrow{{ + NaHC{O_3}}}N{a_2}C{O_3}\)
Câu 36:
Tiến hành cracking 17,4 gam C4H10 một thời gian trong bình kín với xúc tác thích hợp thu được hỗn hợp khí A gồm CH4, C3H6, C2H6, C2H4, C4H8, H2 và C4H10 chưa cracking. Cho toàn bộ A vào dung dịch brom thấy nhạt màu và khối lượng tăng 8,4 gam đồng thời có V lít khí hỗn hợp B (đktc) thoát ra. Đốt cháy hoàn toàn B thu được m gam hỗn hợp CO2 và H2O. Giá trị của m
54,4.
nB = nC4H10 ban đầu = 0,3mB = mC4H10 ban đầu – mAnken = 9Đốt B → nH2O = a và nCO2 = b→ nB = a – b = 0,3mB = 2a + 12b = 9→ a = 0,9 và b = 0,6→ mCO2 + mH2O = 42,6
Câu 37:
Hòa tan hết m gam hỗn hợp X gồm MgO, FeO, CuO và Fe3O4 bằng dung dịch HCl, thu được dung dịch Y. Cho toàn bộ Y tác dụng với dung dịch NaOH dư, thu được (m + 5,85) gam kết tủa. Biết trong X, nguyên tố oxi chiếm 26% khối lượng. Giá trị của m là
20.
Mỗi O sẽ được thay thế bởi 2OH nên:nO = 5,85/(17.2 – 16) = 0,325→ mX = 0,325.16/26% = 20 gam
Câu 38:
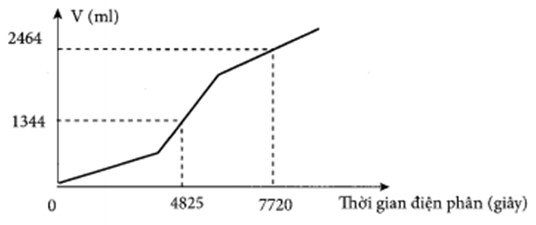
Tiến hành điện phân dung dịch chứa a mol CuSO4 và b mol NaCl bằng dòng điện một chiều có cường độ 2A (điện cực trơ, màng ngăn xốp, hiệu suất điện phân 100%, bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước). Gọi V là tổng thể tích khí (đktc) thoát ra ở cả hai điện cực. Quá trình điện phân được mô tả theo đồ thị sau:
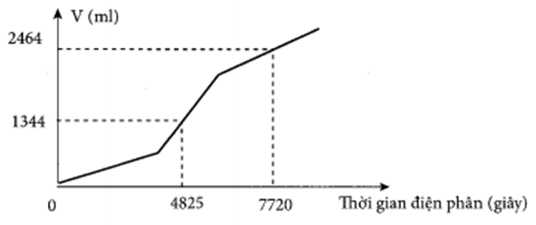
Tỉ lệ a : b là:

Tỉ lệ a : b là:
3 : 8.
Nhìn vào đồ thị, ta tấy quá trình điện phân gồm 3 giai đoạn.

Câu 39:
Cho các phát biểu sau:
(a) Phân tử chất hữu cơ luôn chứa nguyên tố cacbon và hiđro.
(b) Tơ xenlulozơ axetat thuộc loại tơ tổng hợp.
(c) Nước ép của chuối chín không có khả năng tham gia phản ứng tráng gương.
(d) Trong phân tử tripeptit glu-lys-ala có chứa 4 nguyên tử N.
(e) H2N-CH2-CH2-CO-NH-CH2-COOH là một đipeptit.
Số phát biểu đúng là
(a) Phân tử chất hữu cơ luôn chứa nguyên tố cacbon và hiđro.
(b) Tơ xenlulozơ axetat thuộc loại tơ tổng hợp.
(c) Nước ép của chuối chín không có khả năng tham gia phản ứng tráng gương.
(d) Trong phân tử tripeptit glu-lys-ala có chứa 4 nguyên tử N.
(e) H2N-CH2-CH2-CO-NH-CH2-COOH là một đipeptit.
Số phát biểu đúng là
1.
(a) Sai vì theo định nghĩa hợp chất hữu cơ luôn chứa nguyên tố cacbon không nhất thiết chứa hidro.(b) Sai vì đây là tơ bán tổng hợp hay là tơ nhân tạo.(c) Sai vì nước ép của chuối chín có chứa glucozơ nên tham gia phản ứng tráng gương.(d) Đúng vì glu và ala có 2N còn lys có 2N.(e) Sai vì chất này không được tạo bởi 2 \(\alpha \)-aminoaxit.
Câu 40:
Tiến hành thí nghiệm phản ứng màu biure- Bước 1: Cho vào ống nghiệm 1 ml dung dịch protein 10%, 1ml dung dịch NaOH 30% và 1 giọt dung dịch CuSO4 2%.- Bước 2: Lắc nhẹ ống nghiệmPhát biểu nào sau đây đúng?
Có thể thay dung dịch protein trong thí nghiệm trên bằng dung dịch xenlulozơ.
CuSO4 phản ứng với NaOH tạo kết tủa màu xanh lam Cu(OH)2Phản ứng giữa Cu(OH)2 với các nhóm peptit -CO-NH tạo ra sản phẩm màu tím đặc trưng.→ Phát biểu đúng: Sau bước 2, dung dịch xuất hiện màu tím đặc trưng.
Giải thích & Đáp án chi tiết
Câu 1
Đáp án đúng: B
C6H12O6.
Câu 2
Đáp án đúng: D
axit glutamic.
Câu 3
Đáp án đúng: C
Na.
Câu 4
Đáp án đúng: D
KNO3.
Câu 5
Đáp án đúng: A
Amilopectin.
Câu 6
Đáp án đúng: A
HCl.
Câu 7
Đáp án đúng: B
hiđro hóa.
Câu 8
Đáp án đúng: D
Cr.
Câu 9
Đáp án đúng: C
NaNO3.
Câu 10
Đáp án đúng: C
Benzen.
Câu 11
Đáp án đúng: C
Sắt.
Câu 12
Đáp án đúng: C
FeO.
Câu 13
Đáp án đúng: D
AlCl3.
Câu 14
Đáp án đúng: B
HCOOC2H5.
Câu 15
Đáp án đúng: C
Glyxin.
Câu 16
Đáp án đúng: C
10.
Câu 17
Đáp án đúng: D
Be.
Câu 18
Đáp án đúng: B
HCl.
Câu 19
Đáp án đúng: C
Sinvinit.
Câu 20
Đáp án đúng: B
2.
Câu 21
Đáp án đúng: C
CH3COOCH3.
Câu 22
Đáp án đúng: D
1.
Câu 23
Đáp án đúng: D
2,94.
Câu 24
Đáp án đúng: B
0,10.
Câu 25
Đáp án đúng: C
Fe(OH)3, Cu.
Câu 26
Đáp án đúng: D
2.
Câu 27
Đáp án đúng: B
2,24
Câu 28
Đáp án đúng: B
147.
Câu 29
Đáp án đúng: B
0,3 và 33,72%.
Câu 30
Đáp án đúng: A
17.
Câu 31
Đáp án đúng: C
Nhiệt độ sôi của X4 lớn hơn X3.
Câu 32
Đáp án đúng: B
17,72.
Câu 33
Đáp án đúng: B
98,335.
Câu 34
Đáp án đúng: B
3
Câu 35
Đáp án đúng: A
Na2CO3 và NaOH.
Câu 36
Đáp án đúng: C
54,4.
Câu 37
Đáp án đúng: C
20.
Câu 38
Đáp án đúng: B
3 : 8.
Câu 39
Đáp án đúng: D
1.
Câu 40
Đáp án đúng: A
Có thể thay dung dịch protein trong thí nghiệm trên bằng dung dịch xenlulozơ.